XENOTRANSPLANTASYON: Yeni Bir Umut Olma Yolunda
Transplantasyon özellikle son evre organ yetmezliği olan hastalarda ve kanserin seçili türlerinde en iyi tedavi yöntemi olarak görülüyor. Mevcut teknolojilerle bir hayli kolaylaşmasına rağmen bir başka sorun karşımıza çıkıyor: “Donör yetersizliği”. Sadece Amerika Birleşik Devletleri’nde şu an organ bekleyen 124 673 hasta var. Ancak bir yılda yapılan nakil sayısı yaklaşık 30 000. Arz-talep arasındaki bu uyuşmazlık bilim insanlarını farklı organ kaynakları bulmaya itti ve hayvandan insana organ nakli yani xenotransplantasyon üzerine çalışmalar yoğunlaştı.

Tıp biliminde hastaları tedavi etme sürecinde hayvan kaynaklı hücre ve dokuların kullanılması çok da yeni değil. 17. Yy. da Jean Baptiste Denis, koyun kanını insana enjekte ederek ilk kan xenotransfüzyonunu gerçekleştirdi. Bunu, 19. Yy. ın başlarında domuzdan insana kornea nakli takip etti. 1964’te bir hastaya şempanze kalbi nakledildi. Hasta ameliyattan yalnızca birkaç saat sonra öldü. 1984’te babuna ait bir kalp, bir bebeğe nakledildi. Ancak birkaç hafta içerisinde rejeksiyon dolayısıyla bebek hayatını kaybetti. 1993’te Starlz ve ekibi hepatitli bir hastaya bir babundan alınan karaciğeri nakletmiş ve hastada 70 gün boyunca kayda değer bir red reaksiyonu gözlemlememişlerdir. 1994’te Groth ve ekibi ise domuz pankreas hücrelerini enjekte ettikleri 10 diyabet hastasının ömürlerinin uzadığını bildirmiştir.
Tarihinden de anlaşılacağı gibi xenotransplantasyon üzerine pek çok deneme yapılmış ne yazık ki uzun vadede başarılı bir sonuç alınamamıştır. Şüphesiz ki bunun nedeni xenotransplantasyonu engelleyen mekanizmaların, özellikle immünojenik bariyerlerin tam olarak bulunamaması ve aşılamamasıdır. Peki bilinen bu engeller neler?
- Hiperakut reddi: İnsan kanında önceden var olan antikorlar, yeni transplante edilen organın vasküler epiteline bağlanarak pıhtılaşma yaratır. Bunu önlemek adına nakilden önce hastanın antikorları tüketilmiş ve organ daha sonra nakledilmişse de antikorlar nakil sonrası yeniden üretilmiş ve yine rejeksiyon oluşmuştur.
- Akut Vasküler Red: Gecikmiş organ reddi de denir. Saatler içinde olmasa da günler süren bir rejeksiyondur. Damar içi pıhtılaşma ile sonuçlanır.
Bunların haricinde en önemli risklerden biri de enfeksiyondur. Nakil için yapılan immün baskılama yöntemleri hastada enfeksiyon riskini artırmaktadır. Konu hayvandan alınan bir organ olunca bu enfeksiyon riski bambaşka boyutlara taşınmaktadır.
Bilim insanları ise bu engelleri aşmak için kısa ve orta vadeli de olsa birtakım stratejiler üretmişlerdir. Esasen bu stratejiler donör temelli ve alıcı temelli olmak üzere 2 grupta incelenir.
- Donör Temelli Stratejiler: Transgenik Organlar: Canlıların genetiğinin değiştirilmesi özellikle tarımda verimi ve kaliteyi artırmak için sıkça kullanılan, görmeye alıştığımız bir tekniktir. Bu yöntem artık donör canlı üzerinde, alıcı immün sistemini uyaran etkenleri ortadan kaldırmak için de kullanılıyor. Bir grup araştırmacı, immünolojik ifadelerden sorumlu enzimleri kodlayan 1,3 galaktosiltransferaz geninden yoksun ‘Knockout Pigs’ geliştirmiştir.
- Alıcı Temelli Stratejiler: Akut vasküler reddin, kompleman sistemi aktivasyonu sonucu gerçekleştiği düşünülüyor. Alıcıda kompleman sisteminin inhibisyonu sonucu reddin önlenmesi konusunda çalışmalar devam ediyor.
Ayrıca üzerinde çalışılan sayısız farklı immün-baskılayıcı stratejilerden biri de maymunlarda transgenik domuz böbreklerinin transplantasyonundan sonra dalağın alınması işlemidir. Bu yöntemle canlılık süresi 11 haftaya dek çıkarılmıştır.
Heyecan verici bir strateji de nakil öncesinde alıcı canlıya donör olan domuzun kemik iliğinin nakledilmesi vasıtasıyla, nakledilen organa karşı immün cevabı önlemeye yönelik bir nevi kandırmacadır. Donör kemik iliği, alıcının vücudundaki olgun immün hücrelere dönüşebilecek progenitör immün hücreleri içerir. Alıcıdaki bu donör immün hücreleri, nakledilen organa saldıramaz çünkü onu kendi hücresi olarak tanırlar.
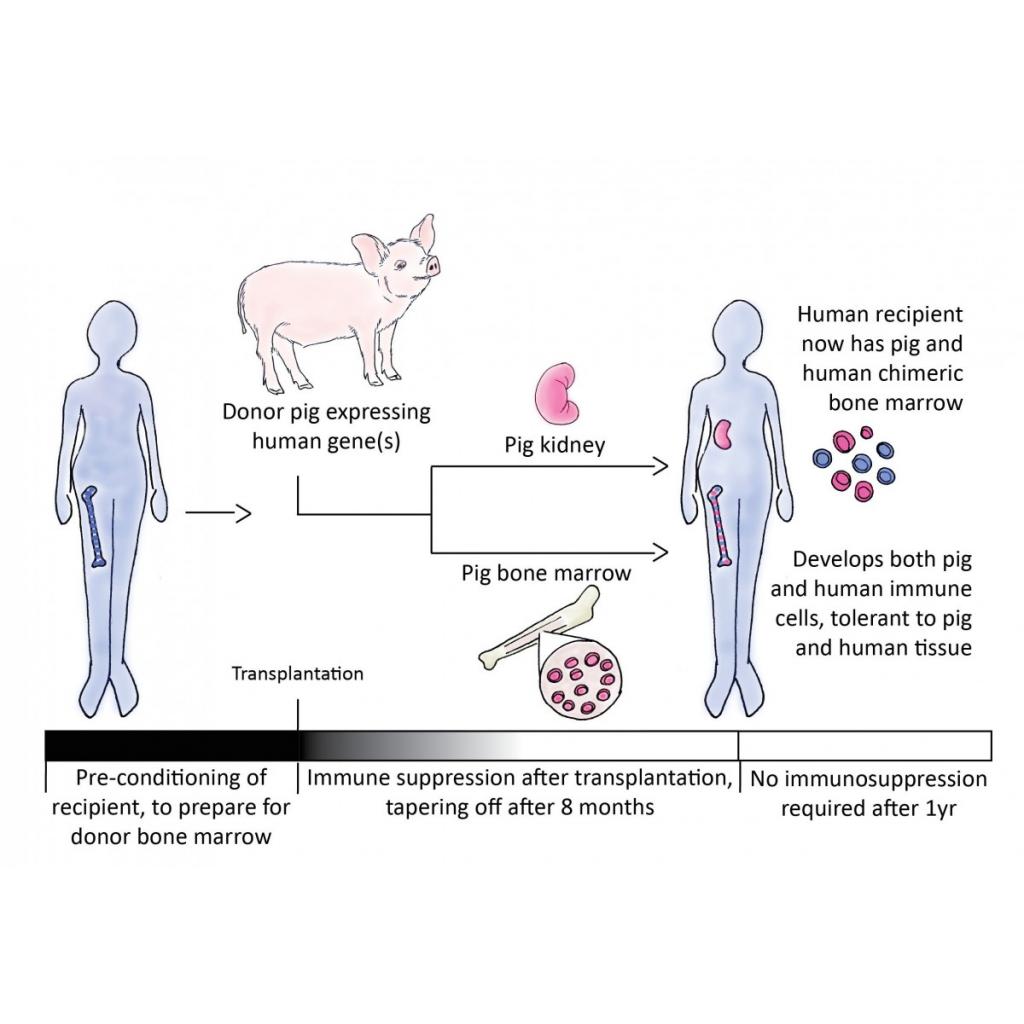
Araştırmacılar insan üzerinde olmasa da hayvanlar üzerinde başarılı çalışmalar yürütmüşlerdir.
Bir grup araştırmacı kimyasal immün baskılama ve donör domuz xenoantijenlerinin azalması vasıtasıyla domuzlardan rhesus maymunlarına transplante edilen böbreğin 435 gün boyunca fonksiyonel olabildiğini gösterdi.
Yine başka bir grup araştırmacı ise domuzlardan babunlara naklettikleri kalplerin tam olarak 945 gün canlı kalabildiğini göstererek hayvan modellerinde xenotransplantasyonun uzun vadeli başarısını göstermiş oldular.

HANGİ HAYVANLAR DONÖR OLARAK TERCİH EDİLMELİ?
Tüm hayvanlar xenotransplantasyon için uygun değillerdir. Çalışmaların tıbbi başarısı açısından seçilen hayvanların insan anatomi ve fizyolojisine yakın olması elzemdir. Ayrıca laboratuvar koşullarında kolay üretilebilmeleri ve etik açıdan kullanılmalarında bir sakıncanın olmaması gerekir. Genetik ve evrimsel anlamda insana en yakın tür maymunlar olmasına rağmen araştırmacılar, primatların taşıdığı yüksek enfeksiyon riski nedeniyle buna uygun olmadığına karar vermişler ve 1990 yılından itibaren primatların xenotransplantasyonda kullanımını yasaklamışlardır. Ayrıca primatlar yüksek oranda zeki canlılar oldukları için laboratuvar ortamında sosyal ve davranışsal gereksinimlerine yanıt vermenin zorluğundan ötürü de kullanılmamaktadırlar.
Domuzlar ise bir kerede yavrulama sayısı, organ boyutlarının insanlarınki ile çok benzer olması, zoonoz ihtimalinin daha düşük olması sebebiyle xenotransplantasyon için en çok tercih edilen hayvanlar olmuşlardır. Ayrıca insanlarda kalp kapakçıklarının değişiminde domuzlara ait kalp kapakçıkları çoktandır uygulanıyor. Ancak bazı dinsel kurallardan ötürü domuzların bu yöntemde kullanımı tartışmalıdır.

KİMERİK XENOTRANSPLANTASYON NEDİR?
“Kimera” modern biyoteknolojide, “bir türe ait kök hücrelerin, başka bir türün bir üyesinin gelişmekte olan embriyo ya da fetüsüne aşılanmasıyla yaratılan canlı” anlamına gelmektedir. Tekniğin amacı immün baskılamaya gerek duymadan alıcı canlıya tamamen uyumlu greftler üretebilmektir. Bu yöntemde donör olan hayvan; istenilen organın gelişeceği, büyüyeceği bir ortam gibi kullanılıyor. Embriyolojik dönemde donör hayvan ilgilenilen doku veya organdan yoksun bırakılıyor. Boş kalan yere, xenogenik hücre de denen alıcı hayvanın pluripotent kök hücreleri enjekte ediliyor ve orada otolog bir organ oluşumu sağlanıyor. İlk başarılı kimeralar Tokyo Üniversitesinden Kobayashi ve ekibi tarafından fare blastositlerine sıçanlardan elde edilen kök hücrelerin enjekte edilmesiyle oluşturuldu. Farelerin vücutlarında sıçan kaynaklı pankreatik parankim başarıyla üretildi.
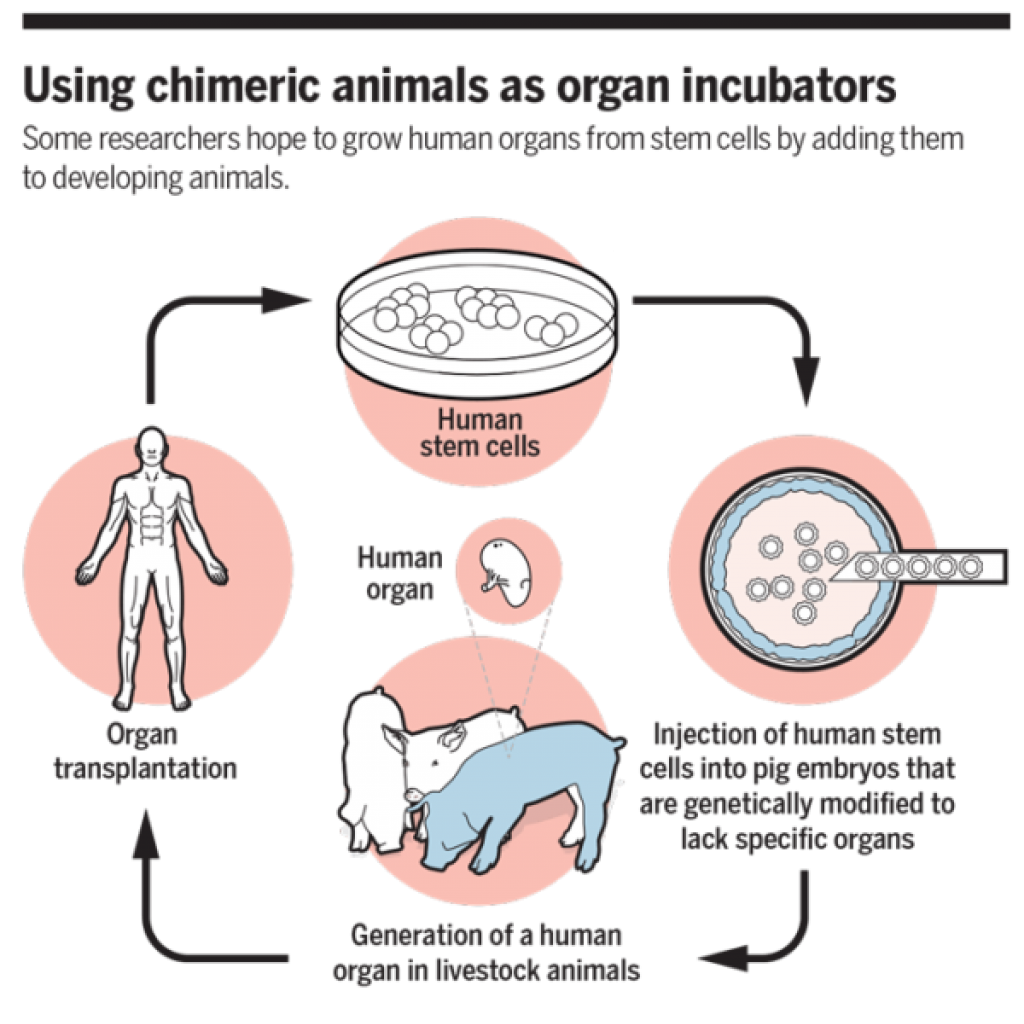
Fetal tamamlanma ise uterus içinde artık fetüs denebilecek büyüklüğe erişmiş hayvana, insan kök hücresi enjeksiyonu ile organ veya doku oluşturma yöntemidir. Örneğin Fisher ve ekibi gestasyonel 40. Günde domuz fetüsüne ait karaciğere insan hepatositlerini enjekte etti. Enjekte edilen bu hepatositler domuz doğduktan sonra da yaşadı ve oluşan kimerik hayvan, xenogenik enjeksiyona karşı daha düşük seviyede bir immün yanıt gösterdi.
PIG ENDOGENOUS RETRO VIRUS (PERV) NEDİR?
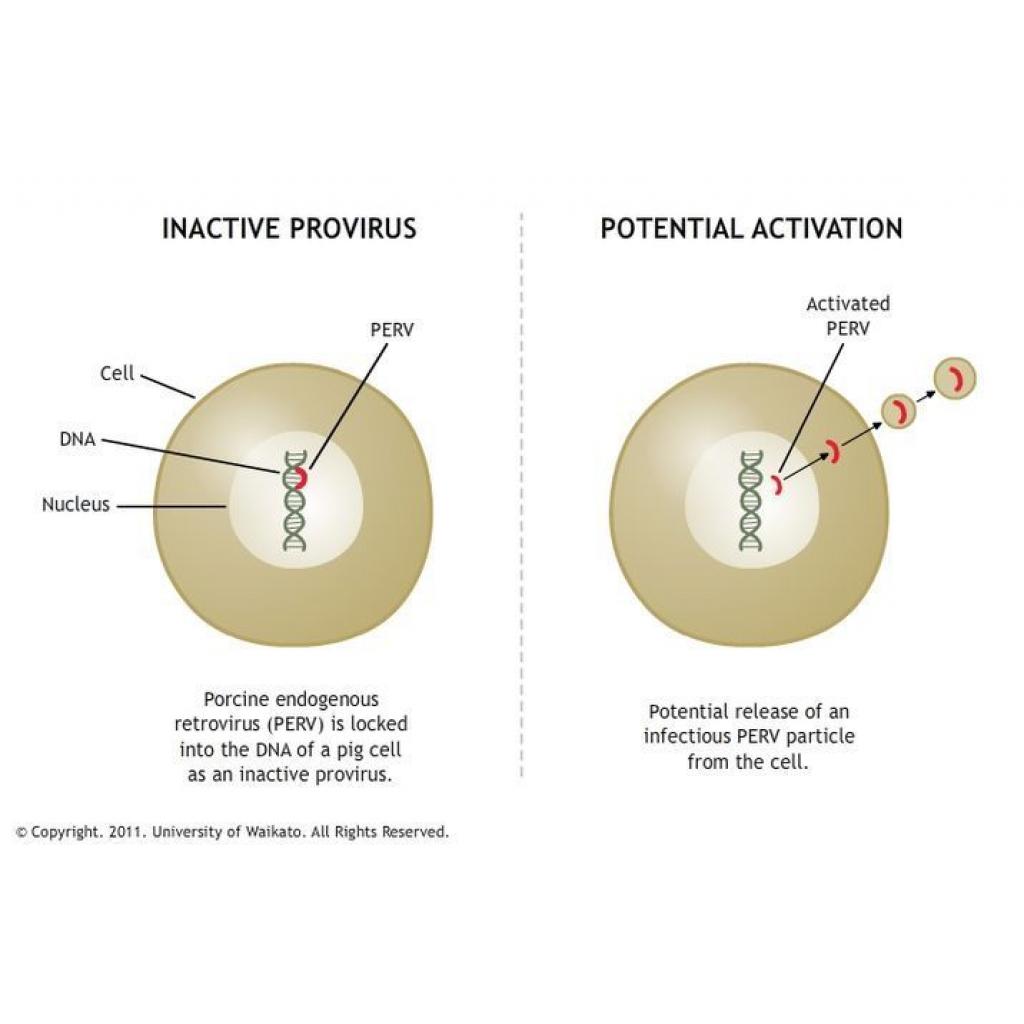
Endojen retrovirüsler insan ve hayvanların kromozomlarına entegre olarak kromozomun bir parçası haline gelen retrovirüs çeşitleridir. Bu dizilerin insan genomunun %8 ini oluşturduğu tahmin edilmektedir. PERV dediğimiz domuz endojen retrovirüs de domuz genomunda taşındığı için xenotransplantasyon uygulamalarında büyük bir risk faktörüdür. İnsanlar için PERV infeksiyonunun riski ilk olarak 1977 de domuz PK15 hücrelerinde tanımlandı. Şu ana kadar domuz hücre veya dokusuna maruz kalan hiçbir hastada PERV’e rastlanmasa da sahip olduğu potansiyel tehlike FDA’nın xenotransplantasyon ile ilgili kılavuzunun revizyonuna neden oldu. Yeni düzenlemeye göre domuz hücre veya dokusu implantasyonu yapılan hastalara, potansiyel PERV infeksiyonu gözlenmesi için tahlil ve prosedür uygulanması gerek.
Bu riski azaltma amaçlı domuzların genomlarındaki PERV bölgeleri dejenere edildi. Bu durum riski azaltabilir ancak tamamıyla yok edemez çünkü farklı PERV bölgeleri arası veya PERV ile insan endojen Retro virüsleri arasında oluşacak olası rekombinasyonlar ortaya yeni virüs tipleri çıkarabilir.
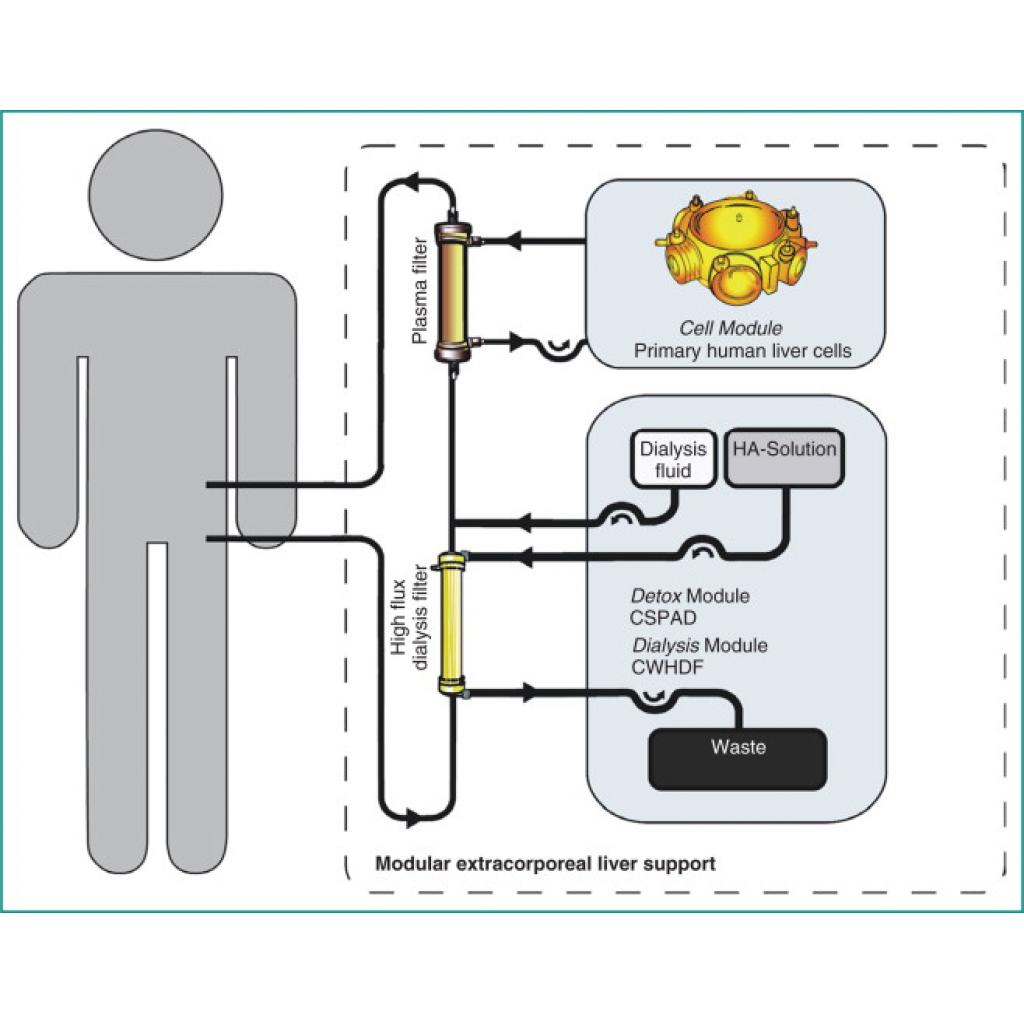
Hayvan hücre ve dokuları sadece xenotransplantasyon için değil başka alanlarda da tedavi amaçlı kullanılmaktadır. Örneğin diyalize benzer bir yöntem ile modifiye edilmiş domuz hepatositleri içeren bir makine, toksik maddelerin eliminasyonunu sağlayarak organ bulunana dek hastanın ömrünü geçici olarak uzatmayı amaçlıyor. Ayrıca Amerika ve Avrupa’da domuz hepatositlerinin kullanıldığı diyaliz makineleri umut verici sonuçlar ortaya koyuyor.
ULUSLARARASI XENOTRANSPLANTASYON BİRLİĞİ (IXA)
IXA, Xenotransplantation’a özel ilgi duyanlar için bir forum sağlamak amacıyla Montreal ’98 Transplantasyon Derneği Kongresi’nde kuruldu. Birlik, görevini “xenotransplantasyonu güvenli, etik ve etkili bir tedavi yöntemi olarak teşvik etmek” şeklinde açıklıyor. Düzenlediği kongrelerle dünya çapında bilim insanlarını bir araya getiren ve son gelişmeleri paylaşma ve tartışma fırsatı sunan birlik, önümüzdeki kongresini bu yıl 10-13 Ekim’de Münih’te yapacak.

Ülkemizde ise İnönü Üniversitesi Karaciğer Nakli Enstitüsü Müdürü Prof. Dr. Sezai Yılmaz Xenotransplantasyon üzerine araştırmalar yürütüyor. Prof. Dr. Yılmaz, yaptıkları çalışmalarla 5 yıl içinde yeni organ kaynaklarının genetik değişikliğe uğratılmış domuzlar olacağını belirtiyor.

Sonuca gelecek olursak xenotransplantasyon; sınırsız organ kaynağı, tekrarlanan seçmeli nakil ve planlı operasyon avantajlarının yanı sıra fizyolojik uyumsuzluk ve enfeksiyon riski gibi potansiyel tehlikeleri ile keşfedilmeyi bekleyen yepyeni bir alan olarak karşımızda duruyor. Şu anda henüz deney aşamasında olsa da kliniğe geçmesi durumunda “Organ Bekleyenler Listesi” belki de tarih olacak…
KAYNAKÇA:
- https://onlinelibrary.wiley.com/doi/full/10.1111/xen.12402
- https://www.ncbi.nlm.nih.gov/pubmed/31310462
- https://www.ncbi.nlm.nih.gov/pubmed/31348017
- https://www.ncbi.nlm.nih.gov/pubmed/31369482
- https://dergipark.org.tr/download/article-file/529826
- “Xenotransplantasyon’un dünü,bugünü ve yarını”, Kadüse, S:5 (2019), s.55-57
- https://www.tts.org/ixa/home
- http://sitn.hms.harvard.edu/flash/2015/xenotransplantation-can-pigs-save-human-lives/
- http://www.hurriyet.com.tr/yazarlar/vahap-munyar/domuzdan-insana-karaciger-nakli-ile-umut-baskenti-olalim-41167276
- http://www.yenimalatya.com.tr/gundem/cok-calisirsak-xenotransplantasyon-nobel-odulunu-malatyaya-h23157.htmlhttps://www.latestly.com/lifestyle/health-wellness/pig-to-baboon-heart-transplant-offers-hope-for-xenotransplantation-in-humans-everything-about-cross-species-organ-transplant-54
- https://www.laboratoryequipment.com/news/2018/08/clearing-xenotransplantation-hurdle-detecting-infectious-disease-pigs
- https://frontiersmag.wustl.edu/2017/12/09/xenotransplantation-and-gene-editing-in-pigs/
- https://www.sciencelearn.org.nz/images/1376-potential-porcine-endogenous-retrovirus-activation
- https://www.sciencedirect.com/topics/medicine-and-dentistry/bioartificial-liver-device
- https://tts.guide/webapp/programme/2
- https://www.omixon.com/brief-history-xenotransplantation/
- http://www.elpergaminense.com/articulo_nuevos_caminos_para_los_clones_la_transgenesis_y_los_xenotransplantes.html
Not: Benim için çok önemli bir kaynak olan Kadüse dergisini hediye eden kıymetli İNÜBAT ailesine teşekkürlerimi sunuyorum.





