CAR-T Hücre Tedavisi: Bugün ve Yarın
Vücudumuzu her türlü “yabancı” nın zararlı etkilerinden korumak üzere tasarlanmış olan immün sistemimiz, kanser odağı geliştirmeye yatkın olan hücreleri ortadan kaldırma kabiliyetine de sahiptir. Her birimizin vücudunda her daim bu savaş sürmekte ve çoğu zaman immün sistem meydandan galip ayrılmaktadır. Fakat immün sistem ne yazık ki namağlup unvanını bazı durumlarda kaybeder ve hepimizin yakından bildiği kanser hücreleri hızla çoğalmaya başlar. Bu hücreler, immün sistemi yanıltmak için çeşitli proteinler eksprese ederler ve kendilerini bir dost gibi göstermekte ustalardır. Araştırmacılar, yıllar içinde immün sistemi kanser hücrelerine karşı daha saldırgan hale getirmenin yollarını aramışlar ve immünoterapi konseptini ortaya çıkarmışlardır. Günümüzde immünoterapi başlığı altında birçok tedavi türü bulunmakta olup, bu yazımda özel olarak değinmek istediğim CAR-T (Kimerik Antijen Reseptör- T) hücre tedavileri bu tedavilerin en yenilerinden bir tanesidir.
CAR-T Hücre Tedavisi Nedir?
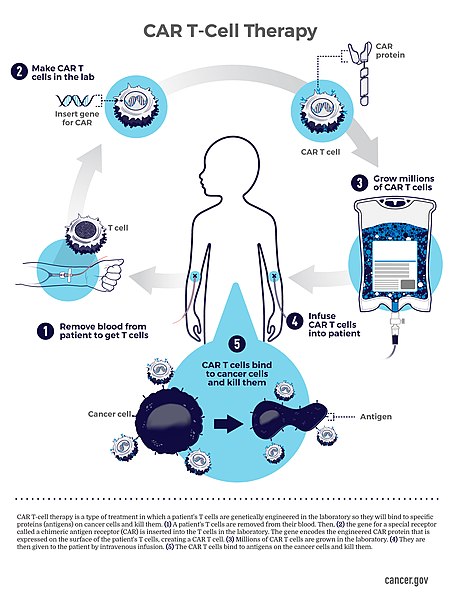
Bu tedavinin temelinde tümör hücreleri üzerindeki proteinleri tanıyabilecek T-hücresi reseptörleri tasarlayarak kanser hücrelerini ortadan kaldırma amacı yatar. CAR-T hücrelerinin elde edilme aşamaları şu şekildedir:
Öncelikle hastanın kanı alınır ve T hücreleri ayrıştırılır. Ardından bu hücreler virüsler veya genetik mühendisliği yöntemleri yardımıyla istenilen kimerik reseptörleri taşıyacak hale getirilirler ve laboratuvar ortamında çoğaltılırlar. Şu an en çok kullanılan yaklaşım CD19 adı verilen hücre yüzeyi proteinine bağlanma yeteneği olan reseptörler üretmektir. Sonrasında hücreler hastaya geri enjekte edilerek bu hücrelerin hastanın vücudunda da çoğalmaları ve kanser hücrelerine karşı etkili olmaları beklenir. Bu tedavi daha çok kan kanserlerine yönelik kullanımda olup 2017’de FDA onayını almış olan 2 ilaç piyasada bulunmaktadır.
Olası Yan Etkiler Nelerdir?
- Covid-19’da da adını sıklıkla duyduğumuz Sitokin Salınım Sendromu ortaya çıkabilmektedir.
- Yukarıda da bahsedildiği üzere CD19’a bağlanan reseptörler üretilmektedir ve CD19 vücudumuzun sağlıklı B hücrelerinde de bulunmaktadır. Bunun bir sonucu olarak hastalarda B-Hücre Aplazisi görülebilmekte ve bir süre İmmünoglobulin tedavisi almaları gerekebilmektedir.
- Serebral Ödem nadir de olsa görülen bir yan etki olarak bir klinik denemede not edilmiştir.
- Birçok hastada görülen fakat kısa sürede ortadan kaybolan konfüzyon, nöbet gibi Nörotoksisite belirtileri görülebilmektedir.
CAR-T hücrelerinin üretim şekli, her hastanın kendi kanından T hücrelerinin elde edilmesi prensibine dayalı olduğundan oldukça zahmetli ve masraflı bir yöntemdir. Bu da bu tedavinin yaygın olarak kullanıma girmesi önündeki en büyük engellerden biri olarak karşımıza çıkmaktadır. Araştırmacılar yan etkisi düşük ve uygun maliyetli alternatif arayışında şimdiden yol kat etmiş durumdadırlar. Bilim camiasında son dönemlerde sıklıkla konuşulan alternatif tedaviler şunlardır:
CAR-T Hücre Tedavisinin Allojenik Uygulanması
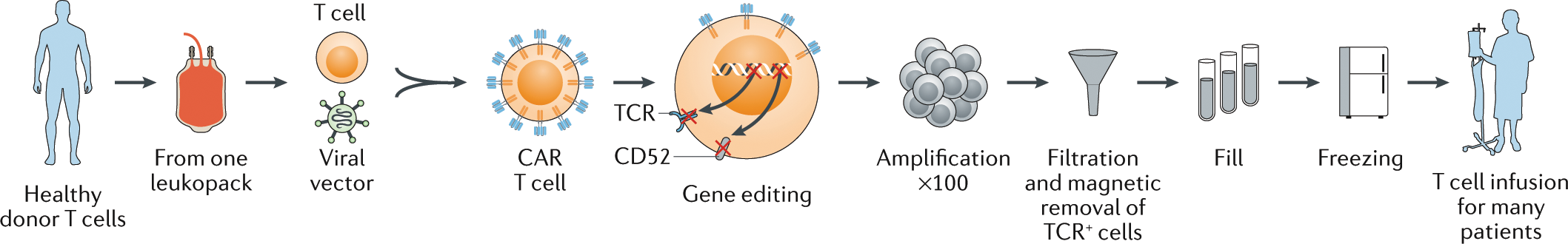
FDA onaylı olan tedaviler hastanın kendi hücrelerinin modifiye edilmesiyle oluşturulmakta ve bu hem oldukça masraflı bir süreç oluşturmakta hem de yaklaşık 3 hafta gibi bir bekleme süresine sebebiyet vermektedir. Ayrıca bazı kan kanserlerinde zaten T hücresi fonksiyonlarında bozulma olduğu gerçeği göz önünde bulundurulduğunda otolog tedavi bazı hastalar için bir seçenek olmanın dışındadır. T hücrelerinin allojenik olarak toplanarak kimerik reseptörlerin oluşturulması ve bu hücrelerin her daim kullanılmaya hazır formda depolanması bu problemlere çözüm olabilecek bir alternatif oluştursa da allojenik tedavinin de bazı kendine özgü riskleri bulunmaktadır. Örneğin; başka bir bireye ait T hücreleri enjekte edildiğinden hastanın bağışıklık sistemi tarafından bu hücrelerin hızla yok edilmesi ihtimal dahilindedir. Ayrıca enjekte edilen T hücrelerinin de alıcının bağışıklık sistemine saldırarak GvHD (Graft Versus Host Disease)’e sebep olma olasılığı bulunmaktadır. CAR-T hücrelerinin ömrünü uzatabilmek için CD52’nin hücre yüzeyinden çıkarılması gibi genetik müdahalelerde bulunularak tedavinin efektifliği arttırılmaya çalışılmaktadır.
Αβ reseptörlü T hücrelerinin GvHD patogenezinde ve transplant rejeksiyonunda temel rol oynadığı bilinmektedir. Bu yüzden αβ T hücreleri dışındaki T hücrelerinin tedavi için kullanımı, reseptör repertuarının daha kısıtlı olması sebebiyle virüs-spesifik hafıza T hücrelerinin kullanımı ve en önemlisi gen editleme yöntemleri kullanılarak αβ T hücrelerindeki reseptörlerin silinmesi ile bu yan etkilerin görülme olasılığını azaltma çalışmaları da yürütülmekte ve bazı klinik denemelerde oldukça umut vadeden sonuçlar alındığı rapor edilmektedir.
CAR-NK Tedavisi
Hastaya daha önceden donör kanından elde edilmiş tedaviyi aktarabilmek için geliştirilmiş yöntemlerden bir tanesi de CAR-NK hücrelerinin geliştirilmesidir. NK olarak kısaltılan “doğal katil” hücrelerimiz periferik kandaki lökositlerin %5-15’ini oluşturmaktadır. Sitotoksik T hücreleri ile benzer bir fonksiyona sahip olup spesifik bir T reseptörüne sahip olmaksızın anti-tümör faaliyetlerini göstermesi yönüyle sitotoksik T hücrelerinden ayrılmaktadırlar. CAR-NK hücreleri, bu özellikleri dolayısıyla GvHD açısından çok daha düşük riske sahiptirler. Salınımına sebep oldukları sitokinlerin sitotoksik T hücreleri kaynaklı salınan sitokinlerden farklı olması Sitokin Salınım Sendromu’na yol açma ihtimallerini oldukça düşürür ve nörotoksisite yine sitokin farklılığının etkisiyle çok daha seyrek görülmüştür. Ayrıca şu an yürütülen bazı gen editleme çalışmaları ile CAR-NK hücrelerinin solid tümörlere karşı da etkin hale getirilebileceği yönünde veriler bulunmaktadır.
Özetle; immünoterapi, hiçbir umut olmadığı düşünülen kanser hastalarına bile umut veren oldukça etkili bir tedavi şekli olmakla birlikte durmaksızın yeni immünoterapi metodları geliştiren tıp dünyası daha fazla hasta için umut ışığı yaratmaya devam etmektedir. Bu tedaviler içerisinde en yenilerden biri olan CAR-T hücre tedavisi, henüz FDA onayını 2017 yılında almış olmasına rağmen daha iyi sonuç verebileceği düşünülen alternatif tedavilerin şimdiden ortaya konmaya başlanmış olması immünoterapinin ne kadar hızlı gelişen bir alan olduğuna dair en canlı kanıtlardan biri olsa gerek. Bu tür yenilikçi tedavilerin daha da çoğalması, immünoterapide ilerleyişin artarak devam etmesi dileğiyle!
KAYNAKÇA
Siegler, E. L., Zhu, Y., Wang, P., & Yang, L. (2018). Off-the-Shelf CAR-NK Cells for Cancer Immunotherapy. Cell stem cell, 23(2), 160–161. https://doi.org/10.1016/j.stem.2018.07.007
Cellular therapies Program. (n.d.), from https://www.dana-farber.org/cellular-therapies-program/car-t-cell-therapy/
Car t cells: Engineering immune cells to treat cancer. (n.d.), from https://www.cancer.gov/about-cancer/treatment/research/car-t-cells
Immunotherapy for cancer. (n.d.), from https://www.cancer.gov/about-cancer/treatment/types/immunotherapy#:~:text=Immunotherapy%20is%20a%20type%20of,a%20type%20of%20biological%20therapy.
Depil, S., Duchateau, P., Grupp, S. A., Mufti, G., & Poirot, L. (2020). ‘Off-the-shelf’ allogeneic CAR T cells: development and challenges. Nature reviews. Drug discovery, 19(3), 185–199. https://doi.org/10.1038/s41573-019-0051-2
Xie, G., Dong, H., Liang, Y., Ham, J. D., Rizwan, R., & Chen, J. (2020). CAR-NK cells: A promising cellular immunotherapy for cancer. EBioMedicine, 59, 102975. https://doi.org/10.1016/j.ebiom.2020.102975
King, A. (2020). Building better CAR-T therapies, from https://www.nature.com/articles/d41586-020-02675-w