GEN TERAPİSİ VE SÖNEN UMUTLAR
GEN TERAPİSİ NEDİR?
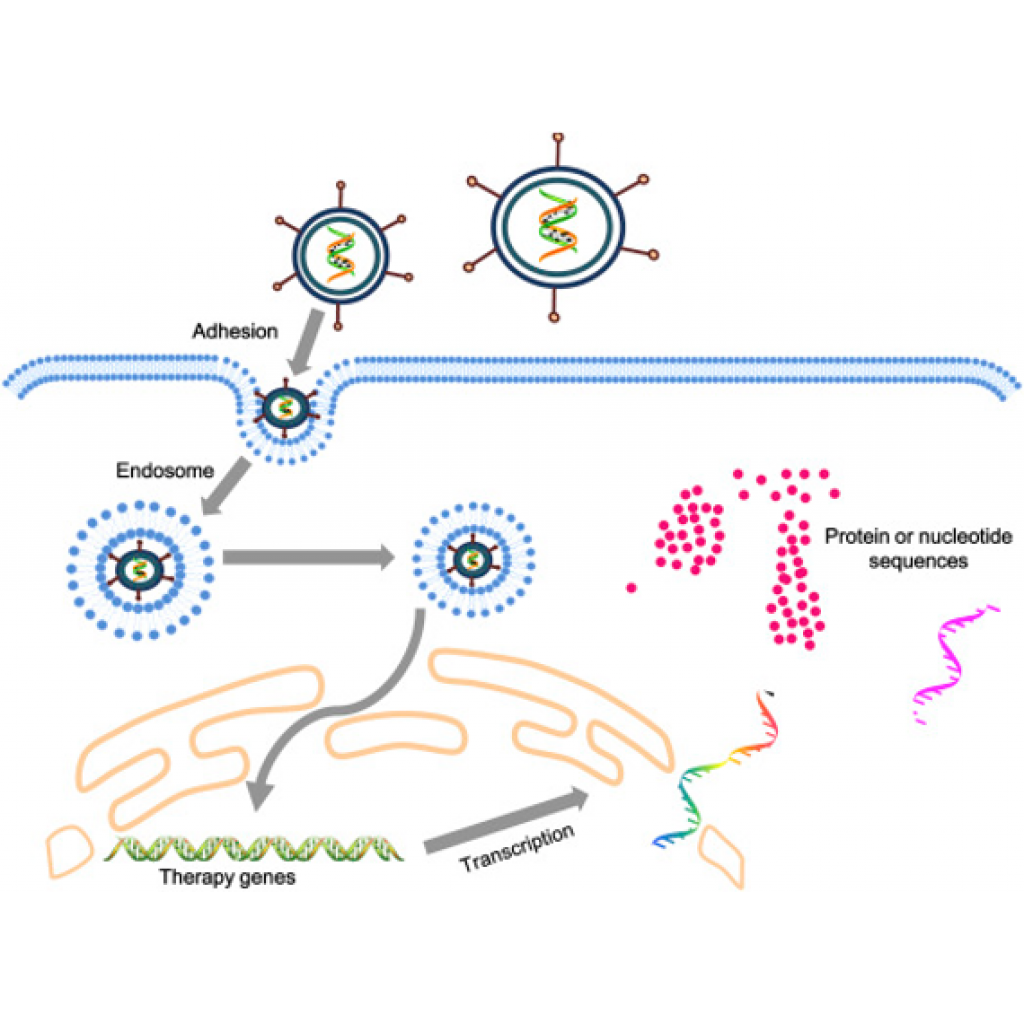
Gen terapisi, gitgide yaygınlaşan ve birçok kişide merak uyandıran bir araştırma konusu haline geldi. DNA’yı anlayabilmek ve kişiye fayda sağlayacak şekilde değiştirebilmek için bilmemiz gereken çok fazla şey var, ancak bu başarıya ulaşabilmek için yapılan çalışmalar birçok gelişmeye imza atıyor. Gen terapisinin önündeki engellerden biri, hastalıkların genetik temelinin karmaşıklığıdır (1). Birçok hastalık, genetik ve çevresel faktörler ile kendini göstermektedir. Buna rağmen hala her yıl binlerce kişiyi etkileyen, kistik fibrozis ve orak hücre anemisi gibi tek gen hastalıkları da bulunmaktadır. DNA dizileme yöntemleriyle elde edilmiş olan bilgiler, bu hastalıkların tedavisinde kullanılabilecek gen dizisi değişimlerinin de anlaşılabilmesini kolaylaştırmıştır. Genom düzenleme yöntemlerinin geliştirilip klinik düzeyde kullanılabilmesi için, bu yöntemlerin doğru diziyi hedefleyebilmesi, verimli işleyebilmesi ve hedef hücrelere/dokulara ulaşabilmesi gereklidir. CRISPR-Cas9 gibi mekanizmaların doğru hücrelerde doğru dizileri doğru şekilde etkilediklerinden emin olunduğu zaman ancak bu mekanizmalar güvenilir bir şekilde terapi haline getirilebilir.

Genom düzenleme süreci sırasında, farklı şekillerde istenmeyen değişiklikler oluşabilir. Örneğin incelenen DNA dizisindeki değişim, istenmeyen bir bölgede yaşanabilir veya enzim doğru bölgeye ulaşsa bile istenmeyen ve hastaya zarar verecek bir mutasyon yaratabilir. Bu yanlışlar çok sık görülmese de bazıları gen terapisi sırasında hastada kanser oluşumuna neden olabilecekleri için tehlikeli de olabilirler (1). Karolinska Enstitüsünde yapılan bir araştırma, CRISPR-Cas9 ile genomları değiştirilen hücrelerde p53 proteiniyle ilgili sorunları ortaya çıkarmıştır (2). p53 proteini, CRISPR-Cas9 mekanizmasının verimini azalttığı için hedef geni istenen şekilde değiştirilmiş hücreleri seçmek, işlevsiz p53 proteinine sahip olan hücreleri seçmek anlamına da gelebilir (3). Dolayısıyla bu hücrelerin kansere neden olabilme olasılığı de değerlendirilmelidir.
JESSE GELSINGER
Jesse Gelsinger, OTCD (ornithine transcarbamylase deficiency/ornitin transkarbamilaz eksikliği) denilen, ornitin transkarbamilaz enziminin eksikliğiyle vücutta amonyak birikmesine neden olan metabolik bir bozukluğa sahipti (4). Erkeklerde daha sık görülen bu hastalığın en ağır formu, yeni doğanlarda daha yaygındır (5). Jesse, hastalığının kendisine verdiği zararın olabildiğince azalabilmesi için beslenmesine çok dikkat ediyordu ve bu şekilde de hastalığıyla baş etmeyi başarabilmişti (6).

Günde neredeyse 50 tane hap alarak bu hastalıkla yaşamını sürdürmeye çalışan Jesse, Pensilvanya Üniversitesindeki araştırmacıların çalışmalarından haberdar olur (4). Kendi hayat kalitesinde büyük bir gelişme görülmesi hedeflenmese bile gelecekte bu hastalığın tedavisinde kullanılabilecek gen terapisinin geliştirilmesine katkıda bulunmak istiyordur; gönüllü olur ve bu amaçla da 1999 yılı Eylül ayında araştırmanın yürütüldüğü yere gider. Bu araştırmacılar, gen terapisi ile OTCD’li farelerde OTC enzimini tekrar işlevli hale getirerek onların yaşamlarını uzatmayı başarmışlardı (4). Jesse’den önce bu klinik araştırmaya katılan diğer kişilerin soğuk algınlığına benzer belirtiler geçirdikleri kaydedilmişti, dolayısıyla kimse Jesse’ninki kadar ağır bir gidişat beklemiyordu. Jesse terapötik Adenovirüs vektörünü aldıktan çok kısa bir süre içinde akciğer, karaciğer ve böbreklerinde tehlikeli problemler yaşadı. Tedaviden dört gün sonra da hayatını kaybetti. Jesse’nin hızlı ve beklenmedik ölümü, toplumun ve bazı proje destekleyicilerinin de gen terapisine bakış açısını olumsuz şekilde etkiledi. CRISPR gibi yöntemlerin geliştirilmesiyle belki de daha güvenli olabilecek gen terapileri üzerine çalışılıyor ancak hala bu terapilerin olası olumsuz etkileri hakkında tartışmalar da devam ediyor.
Jesse’nin neden kaybedildiği araştırılıp anlaşılmaya çalışılırken de bu araştırmanın, Jesse katılmadan önceki dönemde yürütülme şekilleri ve bulguları hakkında da yeni bilgiler ortaya çıktı. Jesse’nin denemelere katılmadan önce diğer hastaların yaşamış oldukları yan etkiler hakkında yeterince bilgilendirilmemesi; denemelerden önce yapılan karaciğer işlev testlerinde Jesse’nin karaciğerinin düşük performans göstermesine rağmen denemelere devam edilmesi, bunlar arasında sayılabilir (3). Jesse’nin kaybedilmesinden hemen sonra elde edilen bilgiler, ilk başta Jesse’nin gösterdiği ölümcül tepkinin rastgele ve öngörülemez olduğunu düşündürmüştü ancak deneme verilerinin daha detaylı incelenmesi, farklı şeylerin de gerçekleşmiş olabileceğini ortaya koydu (6). Örneğin çalışmada bazı deney hayvanlarının ve başka hastaların da ciddi yan etkiler gösterdiğinin, Jesse de dahil olmak üzere denemelere katılan diğer hastalara, oluşabilecek yan etkilerin doğru şekilde söylenmemesi etik tartışmalar yarattı. Jesse’nin ailesi, o tedavi için gönüllü olurken bu durumun onlara açıklanmadığını, dolayısıyla Jesse’nin yeterince bilgi sahibi olmayarak bu işin içine girdiğini söylediler (6). Tüm bunlara ek olarak, Pensilvanya Üniversitesi İnsan Gen Terapi Enstitüsü Başkanı James Wilson’ın yaptığı çalışmada bir çıkar çatışması içinde olduğu da düşünüldü (3). Haberlere göre Wilson’ın Adenovirüslerle yaptığı çalışmaların olumlu sonuçlanmasından Wilson finansal olarak gelir elde edecekti (6). Yani bu durumda klinik çalışmalarında verdiği kararlar da elde edeceği faydayı etkileyecekti. İddiaları reddeden Wilson, Jesse’de görülen durumun öngörülemeyecek bir şey olduğunu ve maddi kazancın verdiği kararları etkilemediğini söylemişti (3). Dolayısıyla Jesse’nin sağlığının bu kadar hızlı bir şekilde kötüye gitmesi ve yaşanan durum hem gen terapisi hem de bu çalışma hakkında akıllarda birçok soruya neden olmuştu.
TECRÜBELER VE GEN TERAPİSİNİN GELECEĞİ
Arkasındaki gerçekler ne olursa olsun, Jesse’nin gen terapisi denemelerinde hayatını kaybetmesi bu alanın birçok açıdan yeniden gözden geçirilmesini ve birçok sınırlandırılmanın yürürlüğe girmesini de beraberinde getirdi. Örneğin Amerika’da FDA (Food and Drug Administration/Amerikan Gıda ve İlaç Dairesi) ve NIH (National Institute of Health/Ulusal Sağlık Enstitüsü) kurumları, daha önceki gen terapi çalışmalarının verilerini incelediklerinde, Jesse’nin ölümünden önceki yedi yıl içerisinde denemelere katılan 691 gönüllünün hayatını kaybettiğini veya hastalandığını, ancak bunlar içerisinden sadece 39 kişinin kısa süre içinde kayıtlara geçirildiğini buldu (3).
Tüm bunlar düşünüldüğünde, gen terapisi hakkında umutsuzluğa kapılmak mümkün olabilir ama aslında durum göründüğünden daha aydınlık. Gen terapisi, Jesse’den önce ve sonra da denenmiş ve birkaç durumda başarılı olmuş veya tedavinin geleceği hakkında değerli bilgiler edinilmesini sağlamıştır. AKİY (Ağır Kombine İmmün Yetmezlik), gen terapisi ile tedavi edilmeye çalışılan ilk hastalıklardandır. Fransa’da 2002 yılında 10 çocukla yapılan klinik denemeler, ilk başta hepsinde başarılı olmuştur ancak ilerleyen yıllarda çocuklardan bazılarında lösemi gelişmesi ve bir tanesinin de hayatını kaybetmesiyle sonlandırılmıştır (7). Bu üzücü kayıplara rağmen denemelere katılan diğer çocuklar tedaviden fayda görmüştür (8). Adenozin deaminaz (ADA) eksikliğinden kaynaklanan genetik bir hastalığa sahip olanAshanti Desilva, diğer tedavi türlerine cevap vermemeye başlamışken gen terapisiyle iyileştirilmiştir (9). Onun gidişatı ve hayatına “normal biri” gibi devam edebilmesi bu denemelere başka çocuklarla da devam edilmesini, başka bir kız çocuğunun daha tedavi edilebilmesini sağlamıştır. Bu güzel gelişmelere ek olarak başka başarılı gen terapisi örnekleri de bulunabilir: Kalıtsal körlük ve hemofili (7) gibi hastalıkların gen terapisi ile tedavisi için de sevindirici sonuçlar elde edilmiştir. Birçok hastalık için de gen terapisinin potansiyeli ve yöntemleri araştırılmaktadır. Gen terapisi; bilimin geldiği bu çağda imkansız bir durum olmak yerine, kullanım stratejileri belirlenmesi, çok dikkatli bir şekilde uygulanması ve doğru noktaya ulaşılabilmesi için de hakkında araştırma yürütülmesi gereken, birçok insanın hayatını değiştirebilecek bir yöntemdir. Dolayısıyla bilim insanlarının bu konuda çalışırken yavaş ve tedbirli ilerlemeleri gerektiği düşünülmektedir (10).
KAYNAKÇA
- Doudna, J. (2020). The promise and challenge of therapeutic genome editing. Nature, 578.
- Haapaniemi, E., Botla, S., Persson, J. et al. (2018). CRISPR–Cas9 genome editing induces a p53-mediated DNA damage response. Nat Med 24, 927–930. https://doi.org/10.1038/s41591-018-0049-z
- Karolinska Institutet. (2018, June 11). Genome-editing tool could increase cancer risk. ScienceDaily. Retrieved July 12, 2020 from www.sciencedaily.com/releases/2018/06/180611133816.htm. Erişim tarihi: 12 Temmuz 2020.
- Science History Institute, ‘The Death of Jesse Gelsinger, 20 Years Later.’ 4 Haziran 2019. https://www.sciencehistory.org/distillations/the-death-of-jesse-gelsinger-20-years-later. Erişim tarihi: 11 Temmuz 2020.
- Genetics Home Reference. (2020). Ornithine transcarbamylase deficiency. https://ghr.nlm.nih.gov/condition/ornithine-transcarbamylase-deficiency. Erişim tarihi: 12 Temmuz 2020.
- NYU High School Bioethics. ‘The Case of Jesse Gelsinger’. https://med.nyu.edu/highschoolbioethics/briefs/jesse-gelsinger. Erişim tarihi: 14 Temmuz 2020.
- University of Utah Genetic Science Learning Center. ‘Gene Therapy Successes’. https://learn.genetics.utah.edu/content/genetherapy/success/. Erişim tarihi: 14 Temmuz 2020.
- Edelstein, M., Abedi, M., & Wixon, J. (2007). Gene therapy clinical trials worldwide to 2007—an update. The Journal Of Gene Medicine, 9(10), 833-842. doi: 10.1002/jgm.1100
- Premier Research, Juliet Moritz. (November 14, 2018). The Four-Year-Old That Changed History’. https://premier-research.com/blog/perspectives-ashanthi-desilva-gene-therapy-trial/. Erişim tarihi: 14 Temmuz 2020.
- McCain, J. (2005). The future of gene therapy. Biotechnology healthcare, 2(3), 52–60.